来源:本文来源网络,版权归相关权利人所有,如侵权,请联系删除
标签归档:稳定性
放射性同位素VS稳定性同位素
放射性同位素VS稳定性同位素
|
|
|
|
|
|
上述产品仅用于科研,不可用于人体实验!
酞菁基ORR电催化剂
为了提高FePc及其衍生物的催化稳定性,常用的策略往往涉及到将酞菁与碳材料复合和高温处理,这些方法虽然能够在一定程度上提高稳定性,但是本征的M-N4大环结构也将在焙烧过程中遭到破坏,影响电子的快速传输并降低催化剂的活性的研究表明,与酞菁外环相连的取代基可以调节中心金属原子的电子结构,实现在稳定性方面的显著提升。同时,具有官能团的FePc衍生物也有能够通过聚合形成高稳定性聚合物。然而,合成聚合物的过程通常涉及繁琐的步骤或苛刻的条件;同时,该方法也很难同时保证活性和稳定性的增强。在ORR活性火山图中,酞菁钴的催化活性低于酞菁铁,但因为酞菁钴不受到与过氧化氢反应的困扰,表现出对ORR良好的稳定性。
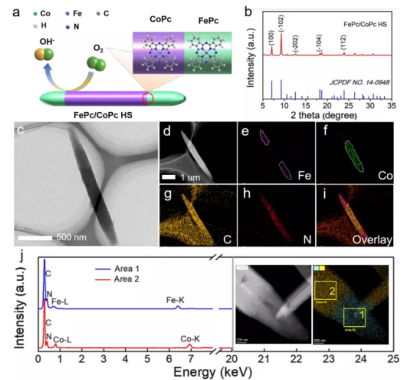
图1 a) FePc/CoPc HS示意图。b) FePc/CoPc HS的XRD图谱。c) FePc/CoPc HS的TEM图像。d – i) FePc/CoPc HS的HAADF-STEM图像以及FePc/CoPc HS对应的EDS能谱。j) 异质界面周围区域1和区域2的EDS谱图。
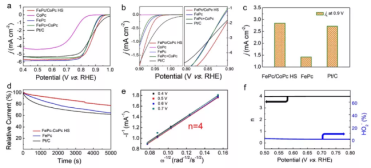
图2 FePc,CoPc,FePc+CoPc,Pt/C和FePc/CoPc HS的a)LSV曲线和b)LSV曲线的局部放大曲线。c)FePc,CoPc和FePc/CoPc HS的动力学电流jk。d)半波电势下的FePc,Pt/C和FePc/CoPc HS稳定性。e)不同转速RDE测试得到的FePc/CoPc HS的K-L曲线。f)RRDE测试计算得到的电子转移数(n)和中间产物产率(HO2-)。
在LSV曲线中(图2a),FePc/CoPc HS的起峰电位达到0.971 V,优于CoPc (0.891 V),FePc (0.958 V) 和 FePc+CoPc (0.952 V);同时,半波电势达到了0.879 V,也远高于其他催化剂。通过计算在0.9 V下的动力学电流(图3c)发现,相比于FePc,FePc/CoPc HS的动力学电流有了>100%的提升。以上结果都证明了异质结构的FePc/CoPc HS展现出优异的电催化活性。在半波电势下测试稳定性(图3d),FePc/CoPc HS 的活性保持率达到了77.4%,超过了FePc (64.2%)和Pt/C (62.6%)。这一结果证明异质结构的设计能够显著提升稳定性。从K-L曲线计算得到ORR的电子转移数为4(图2e),RRDE的结果也能佐证,在整个过程中,中间产物产率极低(图2f),说明FePc/CoPc HS 可以促进ORR反应向4电子过程进行,具有高的反应活性,同时具有较低的中间产物生成率。
三氟乙氧基取代酞菁化合物
苯胺及其季铵化酞菁光敏剂
苯胺酞菁(Zn Pc1)/季铵盐(Zn Pc2)酞菁
含酰亚胺结构超支化酞菁复合材料
酞菁/碳纳米管复合材料
金属酞菁/石墨烯复合材料
酪氨酸修饰的锌酞菁
酞菁-苝酰亚胺功能染料
聚方酸菁功能材料
超支化酞菁锌
磺酸基酞菁/石墨烯静电自组装薄膜
卟啉酞菁的双层化合物
四取代酞菁配合物
酞菁/二氧化硅复合大孔材料
酞菁氧钛单晶有机材料
重氮盐功能化石墨烯/酞菁复合材料
不对称“3+1”类型锌酞菁化合物
手性酞菁-稀土三明治配合物
六羧基双核酞菁钴
酞菁高分子磁性复合材料
酞菁铁有机磁性树脂杂化材料
酞菁铁/纳米铁磁性复合材料
苯乙烯-二乙烯苯树脂负载双核钴酞菁
2,9,16,23-四烷氧基酞菁钴(Ⅱ)
二(磺酸钾基)二(邻苯二甲酰亚胺甲基)酞菁锌
新型侧链取代稀土酞菁配合物
钯酞菁配合物荧光材料
四-α(β)-(4-吡啶氧基)酞菁锌
酞菁铜染料/TiO2纳米粒子异质结LB膜
PA6/酞菁纳米复合材料
SnO2基酞菁敏化纳米复合光催化材料
八异戊氧基酞菁铅旋涂膜
β-磺酸钾基酞菁锌混合物
四-α-(2,2,4-三甲基-3-戊氧基)酞菁钴(镍、铜、锌)
四-α-(2,2,4-三甲基-3-戊氧基)酞菁钒氧
四-α-(2,4-二叔丁基苯氧基)酞菁钒氧
层析硅胶键合酞菁铜
c60富勒烯轴向取代的钛酞菁化合物
四-β-(7-香豆素氧基)酞菁锌(Ⅱ)
四-β-(4-吡啶硫基)酞菁锌(Ⅱ)
α(β)-(2,4-二叔丁基苯氧基)酞菁钴
四-β-(8-喹啉氧基)取代酞菁金属配合物
氧化铁气凝胶纳米粒子酞菁复合材料
稀土酞菁纳米有序复合光电功能材料
三明治型稀土酞菁和氨基取代稀土酞菁
二磺酸基二邻苯二甲酰亚胺甲基酞菁锌
酞菁铜磺酰氯接枝聚苯胺
方酸菁功能材料修饰纳米晶TiO2薄膜电极材料
钴萘酞菁
可溶性亚酞菁
酞菁金属有机框架MOFs
近红外酞菁纳米复合材料
功能化酞菁金属有机骨架
UiO-66型NMOF光敏剂(UiO-66-TPP)
酞菁锌修饰H2L-ZnPc[对三联苯]-4,4’’二羧酸有机配体
H2L-ZnPc/UiO-68-NH2
H2L-ZnPc在H2L-ZnPc/UiO-68-NH2
金属酞菁@金属有机框架催化剂
RHO-[Zn(eim)2](MAF-6)
酞菁功荧光探针
阳离子铝酞菁-血卟啉单甲醚缔合物
酞菁缔合物红区荧光探针
红色荧光探针羧基铝酞菁
阳离子铝酞菁红区荧光探针
四磺基铝酞菁-十四烷基二甲基乙基氯化铵离子缔合物红色荧光探针
阳离子铝酞菁-黏多糖缔合物荧光探针
新型亚酞菁荧光探针
半乳糖/酞菁近红外荧光探针
四硝基铝酞菁荧光探针
