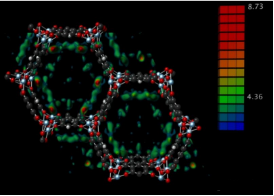
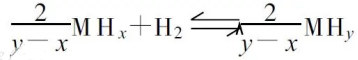常见储氢材料-合金储氢材料/无机物及有机物储氢材料/纳米储氢材料/碳质材料储氢/配位氢化物储氢/水合物储氢
常见储氢材料
合金储氢材料
储氢合金是指在一定温度和氢气压力下,能可逆地大量吸收、储存和释放氢气的金属间化合物。
储氢合金由两部分组成,一部分为吸氢元素或与氢有很强亲和力的元素(A),它控制着储氢量的多少,是组成储氢合金的关键元素,主要是ⅠA~ⅤB族金属,如Ti、Zr、Ca、Mg、V、Nb、Re(稀土元素);另一部分则为吸氢量小或根本不吸氢的元素(B),它则控制着吸/放氢的可逆性,起调节生成热与分解压力的作用,如Fe、Co、Ni、Cr、Cu、Al等。图1列出了一些金属氢化物的储氢能力。
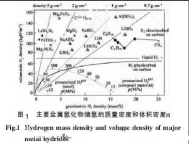
目前世界上已经研制出多种储氢合金,按储氢合金金属组成元素的数目划分,可分为:二元系、三元系和多元系;按储氢合金材料的主要金属元素区分,可分为:稀土系、镁系、钛系、钒基固溶体、锆系等;而组成储氢合金的金属可分为吸氢类(用A表示)和不吸氢类(用B表示),据此又可将储氢合金分为:AB5型、AB2型、AB型、A2B型。
无机物及有机物储氢材料
一些无机物(如N2、CO、CO2)能与H2反应,其产物既可以作燃料,又可分解获得H2,是一种目前正在研究的储氢新技术。如碳酸氢盐与甲酸盐之间相互转化的储氢反应,反应以Pd或PdO作催化剂,吸湿性强的活性炭作载体,以KHCO3或NaHCO3作储氢剂储氢量可达2wt%。该方法的主要优点是便于大量地储存和运输,安全性好,但储氢量和可逆性都不是很好。
有些金属可与水反应生成氢气。例如Na,反应后生成NaOH,其氢气的质量储存密度为3wt%。虽然这个反应是不可逆的,但是NaOH可以通过太阳能炉还原为金属Na。同样,Li也有这种过程,其氢气的质量储存密度为6.3wt%。这种储氢方式的主要难点是可逆性和控制金属的还原。目前,对于Zn的应用较成功。
Li3N的理论吸氢量为11.5wt%,在255℃氢气氛中保持半个小时,总吸氢量可达9.3wt%。在200℃下,给予足够的时间,还会有吸收。在200℃真空(1mPa)下,6.3wt%的氢被释放,剩余的氢要在高温(高于320℃)下,才能被释放。与其他金属氢化物不同的是,在PCT曲线中,Li3N有两个平台:一个有较低的平台压,第二个则是一个斜坡。
有机物储氢技术始于20世纪80年代。有机物储氢是借助不饱和液体有机物与氢的一对可逆反应,即利用催化加氢和脱氢的可逆反应来实现。加氢反应实现氢的储存(化学键合),脱氢反应实现氢的释放。有机液体氢化物储氢作为一种新型储氢技术有很多优点:储氢量大,如苯和甲苯的理论储氢量分别为7.19wt%和6.18wt%;储氢剂和氢载体的性质与汽油类似,因而储存、运输、维护、保养安全方便,便于利用现有的油类储存和运输设施;不饱和有机液体化合物作储氢剂可多次循环使用,寿命可达20年。但这类方法在加氢、脱氢时条件比较苛刻,而且所使用催化剂易失活,因而还在做进一步的研究
纳米储氢材料
纳米材料由于具有量子尺寸效应、小尺寸效应及表面效应,呈现出许多特有的物理、化学性质,成为物理、化学、材料等学科研究的前沿领域。储氢合金纳米化后同样出现了许多新的热力学和动力学特性,如活化性能明显提高,具有更高的氢扩散系数和优良的吸放氢动力学性能。纳米储氢材料通常在储氢容量、循环寿命和氢化–脱氢速率等方面比普通储氢材料具有更优异的性能,比表面积和表面原子数的增加使得金属性质发生变化,具有了块体材料所没有的性质。由于粒径小,氢更容易扩散到金属内部形成间隙固溶体,表面吸附现象也更加显著,因而储氢材料的纳米化已成为当今储氢材料的研究热点。储氢合金纳米化为高储氢容量的储氢材料的研究提供了新的研究方向和思路。
总结了纳米储氢合金优异动力学性能的原因:
(1)大量的纳米晶界使得氢原子容易扩散;
(2)纳米晶具有极高的比表面,使氢原子容易渗透到储氢材料内部;
(3)纳米储氢材料避免了氢原子透过氢化物层进行长距离扩散,而氢原子在氢化物中的扩散是控制动力学性能较主要的因素。
通常情况下Ni-Al合金不具备吸氢特性,采用自悬浮定向流法制备出单相金属间化合物AlNi纳米微粒,纳米AlNi在一定条件下,可在90—100℃实现吸氢–放氢过程,其较大吸附量可达到材料自重的7.3%。
碳质材料储氢
吸附储氢是近几年来出现的新型储氢方法,具有安全可靠和储存效率高等优点。而在吸附储氢的材料中,碳质材料是较好的吸附剂,不仅对少数的气体杂质不敏感,而且可反复使用。碳质储氢材料主要是高比表面积活性炭(AC)、石墨纳米纤维(GNF)、碳纳米管(CNT)。
配位氢化物储氢
配位氢化物储氢是利用碱金属(Li、Na、K等)或碱土金属(Mg、Ca等)与第三主族元素可与氢形成配位氢化物的性质。其与金属氢化物之间的主要区别在于吸氢过程中向离子或共价化合物的转变,而金属氢化物中的氢以原子状态储存于合金中。
表1给出了部分配位氢化物,可以看出它们含有极高的储氢容量,因而可作为优良的储氢介质,其中LiBH4、NaBH4和KBH4已实现了工业化生产。
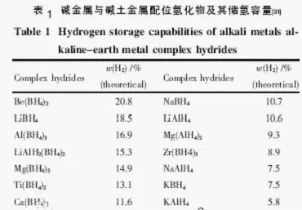
应当指出的是,配位氢化物室温下它的分解速率很低,如LiBH4、NaBH4等金属硼氢化物在干燥或惰性气氛中,要到300℃以上才能分解释放氢气,而且其循环性能的研究也较少。为此以NaAlH4为研究对象,发现催化剂能降低其反应活化能,且Ti4+较Zr4+的催化性能要好。
对于配位氢化物的研究开发,索新的催化剂或将现有催化剂(Ti、Zr、Fe)进行优化组合以改善其低温放氢性能,以及循环性能方面还需做更进一步的研究。[2]
水合物储氢
气体水合物,又称孔穴形水合物,是一种类冰状晶体,由水分子通过氢键形成的主体空穴在很弱的范德华力作用下包含客体分子组成,其一般的反应方程为:
R+nH2O-R·nH2O(固体)十△H(反应热)
水合物通常有3种结构,具体见图2和表2。很多气体或易挥发性液体都能在一定的温度和压力条件下和水生成气体水合物,例如天然气、二氧化碳以及多种氟里昂制冷剂。

水合物储存氢气具有很多的优点:储氢和放氢过程完全互逆,储氢材料为水,放氢后的剩余产物也只有水,对环境没有污染,而且水在自然界中大量存在并价格低廉;其次,形成和分解的温度压力条件相对较低、速度快、能耗少。粉末冰形成氢水合物只需要几分钟,块状冰形成氢水合物也只需要几小时;而水合物分解时,因为氢气以分子的形态包含在水合物孔穴中,所以只需要在常温常压下氢气就可以从水合物中释放出来,分解过程非常安全且能耗少。
wyf 04.